Bugün öğrendim ki: Bilim insanları şizofreni hastası bir insanın bağırsak mikrobiyomunu farelere aktardıklarında, farelerin şizofren benzeri davranışlar sergilemeye başladığını tespit etti.
Şizofreni (SCZ), küresel nüfusun yaklaşık %1'ini etkileyen kronik ve ciddi bir nöropsikiyatrik hastalıktır1 ve SCZ, halk sağlığı üzerinde ağır bir yük oluşturur. Aileye dayalı ve ikizlere dayalı çalışmalardan elde edilen kanıtlar, SCZ gelişiminde yüksek kalıtım oranının %64–%81 arasında olduğunu desteklemektedir2. Birçok genişletilmiş genom araştırması (GWAS), genetik varyantlar ile SCZ riski arasında ilişki olduğunu ortaya koymuştur3,4,5. GWAS'tan elde edilen veriler, glutamaterjik ve dopaminerjik sistemlerin yanı sıra kalsiyum sinyalleşme ve bağışıklık sistemi genlerinin yollarına odaklanıyor gibi görünmektedir ve bu çalışmalar, SCZ'nin patofizyolojisi hakkında da bilgiler sağlamaktadır6. Yine de, GWAS'tan elde edilen bu veriler, SCZ'deki kalıtımın sadece küçük bir kısmını açıklayabilen risk genlerini belirlemiş, nadir varyantlar ve gen-gen etkileşimlerinin ek genetik faktörler olduğu düşünülmektedir. Ayrıca, çevresel faktörler ve genetik varyantlarla etkileşimleri, hastalık fenotipine yol açan nedensel mekanizmaları açıklayabilir. Dahası, SCZ için mevcut tedaviler esas olarak pozitif semptomları hafifletmekte, ancak negatif semptomlar üzerinde daha az etkilidir7. Sonuç olarak, SCZ'nin başlangıcında diğer insan dışı genetik faktörlerin rolünü araştırmak önemli hale gelmiştir. SCZ'nin etiyolojisini ve patolojik mekanizmasını aydınlatmak, yeni ilaç hedefleri aramak, değerli uygulamalara sahiptir ve ayrıca SCZ araştırmalarında kritik bir öncelik olmuştur.
Bağırsak mikroflorası, dışarıdan görünen bir organ olarak kabul edilir ve insan sağlığında önemli roller oynar8,9. Son araştırmalar ayrıca bağırsak mikroflorasının beyin fonksiyonlarını ve konakçı davranışlarını düzenleyebileceğini doğrulamıştır10,11. Birkaç ön klinik çalışma, bağırsak mikrobiyal kompozisyon ve çeşitliliğindeki değişikliklerin SCZ ile ilişkilendirildiğini bildirmesine rağmen12,13,14, bağırsak mikrobiyomunun SCZ patogenezine katkısının rolü hala belirsizdir. Önceki çalışmalar, hem ilk atak ilaç almamış hastaların (FSCZ) hem de SCZ'li ilaç alan hastaların (TSCZ) değiştirilmiş bir mikrobiyomuna sahip olduğunu ve ortaya çıkan klinik ve preklinik çalışmalar, bir disbiyoz bağırsak mikrobiyomunun SCZ ile olası ilişkilerini göstermektedir13,14,15, FSCZ ve TSCZ'nin bağırsak mikrobiyal bileşiminde farklı değişikliklere sahip olduğunu göstermektedir15. Hayvan çalışmalarında, SCZ'li ilaç alan hastalardan germsiz (GF) farelere ve ilaç almayan SCZ'li hastalardan SPF farelere mikrobiyom aktarımı, farklı SCZ benzeri davranışsal fenotipler indüklemiştir13,14. Çalışmalar, GF farelerinin, kalıcı nörogelişimsel yetersizlikler nedeniyle beyin ve davranış üzerindeki mikrobiyom etkilerini incelemek için uygun bir model olmayabileceğini göstermektedir16. SCZ araştırmasının büyük bir zorluğu, özellikle beyin dokuları olmak üzere insan materyallerine erişilememesidir. SCZ üzerine yapılan araştırmalar son on yılda eksik olmasa da, SCZ için uygun bir SPF hayvan modeli hala sınırlıdır.
Bağırsak mikroflorasının hipotalamus-hipofiz-adrenal (HPA) ekseni düzenlediği ve değiştirilmiş HPA ekseni işleminin SCZ'deki nörodejeneratif süreçle ilişkili olduğu bilinmektedir17. Bağırsak mikroflorası ile birçok metabolizma yolu arasındaki ilişki, noradrenalin, dopamin ve serotonin metabolizması ve glutamat-glutamin-GABA döngüsü ve kinurenin metabolizması da dahil olmak üzere incelenmiştir13,14. Önceki çalışmalar esas olarak SCZ patogenezi ve ilerlemesinde metabolizmadaki değişiklikleri değerlendirmeye odaklanmıştır. Artan kanıtlar, epigenetik modifikasyonların gen ekspresyonunu, transkripsiyonunu ve eklemeyi etkileyerek normal biyolojik süreçlerde ve ruhsal hastalıklarda önemli roller oynadığını göstermektedir. Gen ekspresyonunun, transkripsiyonun, eklemenin düzenlenmesi, CNS gelişimini etkilemenin başka bir yoludur5,6,18. Mikrobiyom ve SCZ arasındaki ilişkiyi açıklayan önemli moleküler hedefleri belirlemek gereklidir.
Bu çalışmada, SCZ'li antipsikotik tedavi gören hastaların (SCZF grubu) ve sağlıklı kontrollerin (HCF grubu) bağırsak mikrobiyal toplulukları arasında 16S rRNA gen dizilemesi kullanılarak bir karşılaştırma yaptık. Daha sonra, ilaç almayan hastalardan alınan mikrobiyom kullanılarak yakın zamanda yayınlanan çalışmalarla paralel olarak, SCZ'li antipsikotik tedavi gören hastalardan SPF farelere FMT uyguladık14. Sonuçlarımız, antipsikotik tedavi alan SCZ hastalarında değiştirilmiş bir mikrobiyom olduğunu ve değiştirilmiş bağırsak mikrobiyomunun SPF farelerinde SCZ benzeri semptomlar indüklediğini göstermiştir. RNA dizilemesi ve biyoinformatik analizlerimiz, Nöroaktif ligand-reseptör etkileşimi, bağışıklık ve iltihaplanma sinyal yollarının, farelerde mikrobiyom kaynaklı SCZ benzeri davranışsal anormalliklerle ilişkili olabileceğini ortaya koydu. Ayrıca, verilerimizi ve önceki yayınlanmış SCZ insan beyin dizileme verileriyle yapılan birleşik analiz, Cybb, Gabre, Baiap3 ve Magel2 de dahil olmak üzere dört genin, SCZ benzeri davranışların altında yatan potansiyel moleküler hedefler olabileceğini gösterdi.
**İnsan Konuları**
Bu çalışma protokolü Helsinki Bildirgesi'ne uygun olarak yürütülmüş ve Şangay Jiaotong Üniversitesi Tıp Fakültesi'ne bağlı Şangay Ruh Sağlığı Merkezi Etik Kurulu tarafından onaylanmıştır. Tüm katılımcılar, herhangi bir deneyden önce yazılı bilgilendirilmiş onay vermişlerdir. Bu çalışmada, 20 SCZ ve 15 sağlıklı kontrol (HC) denek, Şangay Ruh Sağlığı Merkezi'nden (Şangay Jiaotong Üniversitesi Tıp Fakültesi'ne bağlı) temin edilmiştir. Tüm hastalar işe alındığında antipsikotik ilaçlar (risperidon, olanzapin, aripiprazol) kullanmaktaydılar. Ayrıca, örneklemeden önce herhangi bir gastrointestinal semptomları olmayan denekler de dahil edilmiştir. Normal ve taze dışkı örnekleri toplandı ve daha sonraki kullanım için -80°C'de donduruldu. Tüm katılımcıların ayrıntılı bilgileri Tablo 1'de sunulmuştur.
**DNA Ekstraksiyonu ve 16S rRNA Gen Dizilemesi**
Mikrobiyal DNA, TIANamp Dışkı DNA Seti (TIANGEN, Şangay, Çin) kullanılarak dışkı örneklerinden çıkarıldı. Bakteri 16S rRNA geni (hiperdeğişken V3-V4 bölgesi), evrensel 16S primerleri (341F/806R) kullanılarak PCR ile çoğaltıldı. PCR, Bio-Rad model C1000 termik siklerleyici (Bio-Rad, Richmond, CA, ABD) kullanılarak gerçekleştirildi. Her örnek için üç tekrarlama yapıldı ve PCR ürünleri Vazyme VAHTSTM DNA Temiz Küreleri (Vazyme Biotech Co., Ltd., Çin) ile saflaştırıldı ve Illumina MiSeq platformunda Şangay Kişisel Biyoteknoloji Co., Ltd. (Şangay, Çin) ve Magigene Biyoteknoloji Co., Ltd. (Guangzhou, Çin) tarafından dizilendi.
Ham diziler, DADA2 eklentisiyle DADA2 işlem hattı kullanılarak kalite filtreleme, gürültü azaltma, birleştirme ve chimera filtrelemesinden geçirildi19. Nadirleştirme analizi, her örnek için dizi sayısı ve ASV'lere dayanarak, dizileme derinliğinin yeterliliğini değerlendirmek için kullanıldı. Alfa çeşitlilik, çeşitlilik indeksi (Shannon, Simpson ve Faith'in Filogenetik Çeşitlilik), zenginlik indeksi (Gözlenen türler ve Chao1) ve eşitlik (Pielou'nun eşitlik) kullanılarak değerlendirildi20. Gruplar arasındaki alfa çeşitlilik, Kruskall Wallis ve Dunn testi kullanılarak karşılaştırıldı. Beta çeşitlilik, ağırlıklandırılmamış_UniFrac mesafeleri kullanılarak analiz edildi21. İki grup arasındaki farklı bol miktarda takson, Doğrusal ayırt edici analiz (LDA) etki büyüklüğü (LEfSe) kullanılarak belirlendi22. Venn diyagramı, genescloud platformu (https://www.genescloud.cn) kullanılarak gruplar arasındaki ortak ve benzersiz ASV'leri karakterize etmek için oluşturuldu.
**Hayvanlar ve Antibiyotik Tedavisi**
Erkek C57BL/6 fareleri (6 haftalık), Şangay JieSiJie Laboratuvar Hayvanları Co., Ltd. (Şangay, Çin) tarafından temin edildi. Tüm hayvan deneyleri yerel hayvan etik kurulları tarafından onaylandı (onay numarası: SV-20201026-02). Fareler rastgele gruplandırıldı ve her 4-5 fare tek kafese SPF koşullarında, 12 saatlik aydınlık/12 saatlik karanlık döngüsü altında konuldu. Uygulama sonrası, önceki raporlara göre başlangıç mikrobiyomunu ortadan kaldırmak için bir antibiyotik kokteyli hazırlandı23. Özetle, farelere 3 gün boyunca 1 mg/kg amfoterisin-B oral gavajı yapıldı ve ardından her fareye 7 gün boyunca 50 mg/kg vancomycin, 100 mg/kg metronidazol, 100 mg/kg neomisin trisülfat ve 1 mg/kg amfoterisin-B'den oluşan bir antibiyotik kokteyli verildi. Ampisilin, fareler için 1 g/L konsantrasyonda içme suyuna çözüldü. Antibiyotik kokteyli solüsyonu hazırlandı ve taze kullanıldı ve tüm antibiyotikler Sigma-Aldrich (Şangay, Çin) ve Macklin Biyokimya Teknolojisi (Şangay, Çin) tarafından satın alındı.
**FMT Deneyleri**
Önceki çalışmalarda açıklandığı gibi20,23, rastgele seçilen beş SCZ hastasından ve beş demografik olarak eşleştirilen sağlıklı kontrole ait dışkı örnekleri FMT için hazırlandı. Özetle, dışkı örnekleri steril fosfat tamponlu solüsyon (PBS) ile süspansiyon haline getirildi ve ardından 100 µM elekten geçirildi. Toplanan süpernatan 6000×g'de 15 dakika santrifüj edildi. Dışkı mikrobiyomu gliserin-PBS'de süspansiyon haline getirildi ve nakil için kullanıldı24. 3 hafta boyunca antibiyotik kokteyli alan her fareye, 3 hafta boyunca haftada iki kez 200 µL hacminde mikrobiyom süspansiyonu oral gavaj yoluyla verildi.
**Davranış Testleri**
**Açık Alan Testi**
Açık alan testi (OFT; kendiliğinden aktivite, uyarılabilirlik ve anksiyete benzeri davranışları yansıtır) 27.5 cm × 27.5 cm'lik bir davranış test kutusu içerisinde gerçekleştirildi ve serbestçe keşfetmeye bırakıldı. Her bir farenin hareketi, video kamerasıyla 5 dakika boyunca kaydedildi ve bu çalışmada toplam seyahat mesafesi, ortalama hız ve süre değerlendirildi.
**Yüksek Platformlu Labirent Testi**
Yüksek platformlu labirint testi (EPM; anksiyete benzeri davranışları yansıtır) cihazda, önceki çalışmaya göre küçük değişikliklerle iki açık ve iki kapalı koldan oluşan bir cihazda gerçekleştirildi25. 29 cm uzunluğunda ve 8 cm genişliğinde dört kol ve 17 cm yükseklikte bir labirint vardı. Her bir fare çapraz kesime yerleştirildi ve 5 dakika boyunca aktif olarak erişime bırakıldı. Açık kolda harcanan daha az zaman ve açık kollara daha az giriş, artan anksiyeteyi yansıtır. Bu çalışmada açık kolda aktivite süresi ve toplam açık kola giriş sayısı kaydedildi.
**Zorunlu Yüzer Testi**
Zorunlu yüzer testi (depresyon ve anhedoni benzeri davranışı yansıtır) Porsolt vd. tarafından açıklandığı gibi gerçekleştirildi26, bazı değişikliklerle. Fareler 18 cm çapında ve 25 cm yüksekliğinde bir kap içerisine yerleştirildi. Test süreleri 5 dakika sürdü. Fare, sadece başını suyun üstünde tutmak için küçük hareketler yaparak hareketsizce yüzer kaldığında hareketsiz kabul edildi. Her bir fare için hareketsizlik süresi kaydedildi ve analiz edildi.
**Toplumsal Etkileşim Davranışları**
Sosyallik testinde (sosyallik, sosyal yenilikçilik ve sosyal hafızayı yansıtır), her bir fare üç odalı bir kutuda, odalar arasında açıklıklar bulunan bir yerde konumlandırıldı. Üç Odalı Sosyallik Testi (TCST), ardışık üç denemeden oluşuyordu: deneme 1, fareler odaları 5 dakika boyunca keşfetmeye bırakıldı; deneme 2, sosyal yetenek (bölüm I, yabancı bir fare - fare 1- bir odaya yerleştirildi ve test faresi üç odayı 10 dakika boyunca keşfetmeye bırakıldı, yabancı fare ile boş kafes arasında doğrudan temas süresi kaydedildi). deneme 3, sosyal yenilikçilik tercihi ve sosyal hafıza (bölüm II, yabancı bir fare - fare 2, bölüm I'den fare 1'in karşı tarafındaki odaya yerleştirildi, test farenin yeni yabancı fare ile ve önceki yabancı fare ile doğrudan temas süresi kaydedildi).
**RNA-dizileme kitapçıklarının hazırlanması ve dizilemesi**
Farklı gruplardan alınan farelerin tüm beyin örneklerinden toplam RNA çıkarıldı. Kitapçık yapım ve dizileme, VAHTS mRNA-dizileme V3 Kitapçık Hazırlama Seti (Illumina, San Diego, CA, ABD) kullanılarak gerçekleştirildi. Kalite, NanoDrop Spektrofotometresi (Thermo Fisher Scientific, MA, ABD) kullanılarak değerlendirildi. RNA dizilemesi, Illumina novaqseq pe150 üzerinde yapıldı. Veriler, HISAT2 yazılımı, DESeq paketi, topGO ve clusterProfiler kullanılarak işlendi ve analiz edildi. DEGenler, p<0,05 ve |log2FoldChange|>1 kesme değerleri kullanılarak belirlendi. DEGenler için KEGG ve GO analizleri topGO ve clusterProfiler kullanılarak gerçekleştirildi.
**RNA ekstraksiyonu ve nicel gerçek zamanlı PCR deneyleri**
Yukarıda açıklandığı gibi farklı gruplardan tüm beyinden toplam RNA çıkarıldı ve cDNA, cDNA Sentezi Seti (Takara, Dalian, Çin) kullanılarak sentezlendi. Nicel gerçek zamanlı PCR (qPCR), önceki çalışmamıza göre gerçekleştirildi. Özetle, 20 µL PCR karışımı, 10 µL SYBR qPCR Ana Karışımı (Vazyme, Nanjing, Çin), 2 µL cDNA şablonu, 1 µL ileri primer ve 1 µL ters primer ve 6 µL su içerir. PCR reaksiyonu 95°C'de 30 saniye, ardından 40 döngü 95°C'de 10 saniye, 60°C'de 30 saniye gerçekleştirildi. Veriler 2−△△Ct yöntemi kullanılarak hesaplandı. Kullanılan primerler Ek Bilgi 1'de listelenmiştir. Tüm qPCR amplifikasyonları üçlü olarak ve üç kez tekrarlandı.
**İstatistiksel Analiz**
İki grup arasındaki anlamlı farklılıklar, Student t testi kullanılarak analiz edildi. Grafikler, GraphPad Prism 8 (GraphPad Software, CA, ABD) ve Origin 2019b (OriginLab, MA, ABD) yazılımı kullanılarak oluşturuldu ve ortak veri analizleri gerçekleştirildi. p değeri <0,05 anlamlı olarak kabul edildi.
**Olgu ve Kontrollerin Özellikleri**
Bu çalışmaya 20 SCZ hastası ve 15 sağlıklı kontrol (HC) dahil edildi. Bu hastaların %75'i erkek, %25'i kadın; kontrollerin ise %80'i erkek, %20'si kadındı. Hastaların ortalama yaşı 38,7, kontrollerinki ise 39,5 idi. Yaş, cinsiyet ve vücut kitle indeksi (VKİ) açısından olgular ve kontroller arasında istatistiksel olarak anlamlı bir fark bulunmadı (p>0,05). Tüm SCZ hastaları antipsikotik tedavi görüyordu ancak örneklemeden bir ay önce herhangi bir antibiyotik veya probiyotik kullanmamışlardı.
**SCZ'li hastalarda daha düşük bağırsak bakteri çeşitliliği**
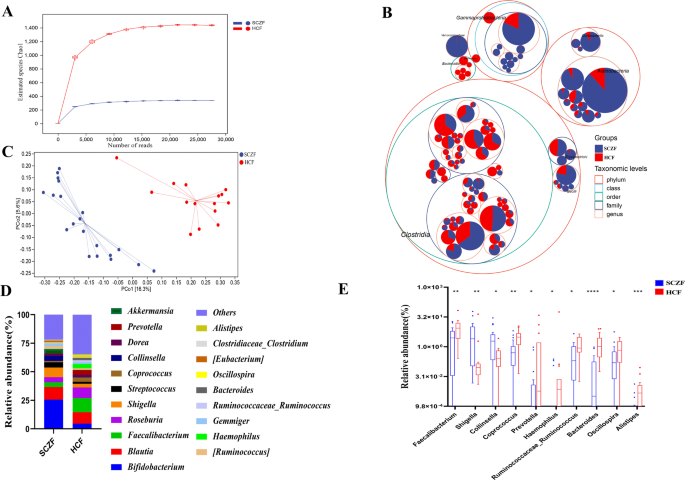
Ortalama olarak, örnek başına 43572 yüksek kaliteli tekil olmayan okuma elde ettik. Örneklerin nadirleştirme analizi, her grupta ASV zenginliğinin doyuma ulaştığını (Şekil 1A) ve SCZF grubunda HCF grubuna göre önemli ölçüde azaldığını gösterdi. Altı farklı endekse göre hesaplanan bağırsak mikrobiyal çeşitlilik, SCZF ile HCF arasında önemli ölçüde azaldı (p<0,001; Şekil S1A ve Tablo S2). Farklı seviyelerde taksonların genel bolluğunu gösteren paketlenmiş dairelerdeki taksonomik ağaç, SCZF ve HCF arasında taksonların bolluğu ve dağılımında belirgin farklılıkları ortaya koydu (Şekil 1B). Beta çeşitliliği göstermek için ana koordinat analizi (PCoA) yapıldı ve sonuçlar, her iki grup arasında bağırsak mikrobiyal topluluklarında önemli bir ayrım olduğunu gösterdi (Şekil 1C). Venn diyagramı, her iki grup arasında 774 ASV'nin ortak olduğunu, 2860 ASV'nin ise sadece SCZF grubuna özgü olduğunu ortaya koydu (Şekil S1B). Bu bulgular, SCZ'li hastaların bağırsak mikrobiyal topluluğunun düşük çeşitlilikle karakterize edildiğini gösterdi.
**SCZ'li hastalarda bağırsak mikrobiyom disbiyozunun özellikleri**
SCZF ve HCF arasındaki bağırsak bakteriyel mikrobiyomun bakteri bileşimi ve bolluklarını daha detaylı olarak karşılaştırdık. Firmicutes, Actinobacteria ve Proteobacteria filumlarının ortalama olarak sırayla %93,4'lük dizilerin temsil edildiğini ve hem SCZF hem de HCF'de üç önde gelen bakteri olduğunu bulduk (Şekil S1C). Filum düzeyinde, Firmicutes, Bacteroidetes ve Tenericutes önemli ölçüde azalırken, Actinobacteria ve Proteobacteria SCZF'de HCF'ye kıyasla önemli ölçüde arttı (Şekil S1D ve Tablo S3). Cins düzeyinde, Bifidobacterium, Blautia ve Shigella, SCZ'li hastaların bağırsak mikrobiyomunda baskın konuma sahipken, Faecalibacterium, Blautia ve Roseburia, sağlıklı kontrollerde baskın konuma sahipti (Şekil 1D). HCF'ye kıyasla, Shigella ve Collinsella olmak üzere yalnızca iki cins arttı, Faecalibacterium, Coprococcus, Prevotella, Haemophilus, Ruminococcaceae_Ruminococcus, Bacteroides, Oscillospira ve Alistipes olmak üzere sekiz cins ise SCZF'de azaldı (tüm p<0,05; Şekil 1E, Tablo S4). Bunlardan Faecalibacterium, Coprococcus ve Bacteroides, konakçının enflamatuar yanıtında önemli anti-enflamatuar etkiler sergileyen kısa zincirli yağ asitleri (SCFAs) üretmek için gereklidir27. Ayrıca, Collinsella ve Escherichia-Shigella'nın çeşitli hastalıklarda esas olarak pro-enflamatuar etkiler sergilediği bildirilmiştir28. Dolayısıyla, SCFA üreten bakterilerde azalma ve pro-enflamatuar bakterilerde artış, SCZ'li hastalardaki enflamatuar yanıtın içinde yer alabilir.
Bu takson bolluğundaki değişikliklerin hiyerarşik kümelemesi, SCZ'li hastalarda sağlıklı bireylere göre farklı kümeler gösterdi (Şekil 2A). SCZF ve HCF grupları arasındaki bağırsak mikrobiyom bileşimindeki ve belirli taksonomik biyobelirteçlerdeki farklılıkları belirlemek için, LEfSe ve metagenomeSeq analizlerini daha ayrıntılı olarak gerçekleştirdik. LEfSe analizi, iki grup arasındaki bakteri taksonlarının göreceli bolluğunda önemli farklılıklar olduğunu gösterdi (Şekil 2B). MetagenomeSeq analizi, SCZF'de yaklaşık 10 ASV'nin önemli ölçüde zenginleştirildiğini ve bu ASV'lerin esas olarak cins düzeyinde Bifidobacterium, Collinsella, Blautia, Shigella ve Acinetobacter'e ait olduğunu gösterdi (Şekil 2C). Ayrıca, tahmin edilen farklı metabolizma yolunun ve bağırsak bakterilerinin ilişkisini analiz ettik ve sonuçlar, Nesterenkonia, Bacteroides, Acinetobacter, Shigella, Burkholderia, Brevundimonas, Pseudomonas, Agrobacterium, Cupriavidus ve Acidovorax'ın göreceli bolluğuyla on iki metabolizma yolunun önemli ölçüde ilişkilendirildiğini ortaya koydu (Şekil 2D).
**SCZ'li hastalardan dışkı nakli, alıcı farelerde SCZ benzeri davranışlar indükler**
SCZ benzeri davranışsal semptomların bozulmuş bağırsak mikrobiyomuyla ilişkilendirilebileceğini belirlemek için, SPF farelerde FMT deneyleri gerçekleştirdik. OFT deneyinde, SCZ dışkı mikrobiyomuna sahip fareler hiperkinetik davranış sergiledi (artmış toplam seyahat mesafesi, Şekil 3A; artmış ortalama hız, Şekil 3B) ve artmış anksiyete gösterdi (merkez alanda harcanan zaman azaldı, Şekil 3C). EPM testinde, SCZ dışkı mikrobiyomuna sahip farelerde, dışkı mikrobiyomu alınmış farelere kıyasla açık kolların giriş sayısı ve açık kolların harcanan zamanı önemli ölçüde azaldı (Şekil 3D, E), bu da anksiyete benzeri davranış olduğunu gösterdi. Zorunlu yüzer testinde ise iki grup arasında bir fark gözlenmedi (Şekil 3F). Sosyallik testinde, HC dışkı mikrobiyomuna sahip fareler, yabancı bir fare yerleştirilen odayı boş bir odaya göre daha fazla süre keşfettiler; ancak SCZ dışkı mikrobiyomuna sahip fare grubunda bu anlamlılık HC grubuna göre önemli ölçüde daha düşüktü (p<0,0001) (p=0,0392; Şekil 3G). Benzer şekilde, HC dışkı mikrobiyomuna sahip fareler, tanıdık bir fareye göre yeni bir fareyi daha fazla süre keşfettiler; ancak SCZ dışkı mikrobiyomuna sahip fare grubunda yeni ve tanıdık bir fareyi keşfetme süreleri arasında bir fark gözlenmedi (Şekil 3H). Genel olarak, bu davranış test sonuçları, hiperaktivite, artmış anksiyete, bozulmuş sosyal etkileşim ve hafıza bozuklukları da dahil olmak üzere SCZ benzeri davranışların, SCZ'li hastalardan bağırsak mikrobiyomunun SPF farelere nakledilmesiyle kısmen yeniden canlandığını gösterdi.
**SCZ veya HC dışkı mikrobiyomuyla nakledilen alıcı farelerdeki bağırsak mikrobiyom bileşimi**
SCZ'li hastaların benzer bağırsak mikrobiyal özelliklerinin SCZ dışkı mikrobiyomuna sahip farelerde başarıyla tekrarlanıp tekrarlanmadığını belirlemek için, SCZ veya HC dışkı mikrobiyomuyla nakledilen farelerin dışkısındaki bağırsak mikrobiyom bileşimini 16S rRNA dizilemesiyle analiz ettik. PCoA, SCZ ve HC dışkı mikrobiyomuna sahip fareler arasında belirgin bir ayrım olduğunu ortaya koydu (Şekil 4A). Venn diyagramı, bağışçının dışkısında bulunan 156 cinsin %36'sının alıcı farelerin bağırsak mikrobiyomunda da bulunduğunu gösterdi (Şekil 4B). SCZ ve HC dışkı mikrobiyomuna sahip fareler arasında farklı olan özellikli bağırsak bakteri mikroplarını belirlemek için rastgele orman analizi gerçekleştirildi. MDA değerleri en yüksek olan 15 bakteri cinsinin sıralaması Şekil 4C'de sunulmuştur. Bunların arasında, Odoribacter, Helicobacter, Corynebacterium_1, Ruminococcaceae_UCG-013, Paraprevotella, ve Ruminiclostridium_6 ve Ruminiclostridium olmak üzere yedi cins SCZ dışkı mikrobiyomuna sahip farelerde daha bolken, geri kalan altı cins (Alistipes, Lactobacillus, Christensenella, Erysipelatoclostridium, Parabacteroides ve Bacteroides) HC dışkı mikrobiyomuna sahip farelerde daha boldu (Şekil 4D). Alistipes'in, SCZ'li hastaların veya SCZ dışkı mikrobiyomuna sahip farelerin kontrol gruplarına göre benzer bir eğilim gösterdiğini belirtmek önemlidir (Şekil 1D ve 4D). Önceki çalışmalar, Alistipes'in SCFA üreterek, triptofan ve GABA'yı etkileyerek SCZ ve diğer ruhsal hastalıklar da dahil olmak üzere çeşitli ruhsal hastalıklarla ilişkili olduğunu bildirmiştir27,29,30. Bu sonuçlar, SPF farelerin bağırsaklarının SCZ'li hastalardan veya sağlıklı kontrollerden alınan dışkı mikrobiyomu ile FMT yoluyla yeniden kolonize edilebileceğini ve SCZ'de rol alan kilit cinsin Alistipes olabileceğini desteklemektedir.
**SCZ dışkı mikrobiyomuna sahip farelerin beyinlerinde düzensiz transkripsiyonel yanıt**
SCZ dışkı mikrobiyomuyla nakledilen farelerdeki davranışsal fenotiplerin altında yatan moleküler mekanizmaları karakterize etmek için, SCZ ve HC dışkı mikrobiyomuna sahip farelerden alınan tüm beyin örneklerinde RNA-dizileme çalışması gerçekleştirdik ve PBS'yi kontrol grubu olarak belirledik. Venn diyagramı, SCZ vs HC ve HS vs PBS grupları arasında 34 DEGen'in örtüştüğünü, ancak sadece 85 DEGen'in SCZ vs HC grubuna özgü olduğunu ortaya koydu (Şekil 5A). Isı haritası, SCZ ve HC dışkı mikrobiyomuna sahip fareler arasında transkriptlerde önemli farklılıklar olduğunu gösterdi (Şekil 5B). Beklendiği gibi, sağlıklı insandan alınan dışkı mikrobiyomu ile SPF farelere FMT uygulanması fare beyin transkriptomunda değişiklikler oluşturdu (Şekil S2). Bu etkileşim faktörünü dışlamak için, SCZ ve HC dışkı mikrobiyomuna sahip fareler arasındaki DEGen fonksiyonlarını keşfetmek için yalnızca 85 DEGen kullanıldı. İlk 20 GO terimi, esas olarak SCZ dışkı mikrobiyomuna sahip farelerin beyninde nöropeptit hormon aktivitesi, reseptör düzenleyicisi ve reseptör ligand aktivitesi, bağışıklık sistemi süreci içermekteydi (Şekil 5C). Biyoinformatik analizler, alıcı fare beyinlerindeki ilk 20 zenginleştirilmiş yolun esas olarak Nöroaktif ligand-reseptör etkileşimi, Fenilalanin metabolizması ve Histidin metabolizması ve Sitokin-sitokin reseptör etkileşimi içerdiğini gösterdi (Şekil 5D ve Tablo S5). Ayrıca, beş DEGen, qPCR kullanılarak daha detaylı olarak doğrulandı ve sonuçlar RNA-dizileme verileriyle uyumluydu (Şekil 5E).
**SCZ hastalarının ve dışkı mikrobiyomuyla nakledilen farelerin beyinlerindeki transkriptomların örtüşmeleri ve farklılıkları**
SCZ hastaları ve FMT fare modeli arasındaki ilişkiyi incelemek için transkripsiyonel özelliklerini karşılaştırmak üzere daha detaylı biyoinformatik analizler gerçekleştirdik. Venn diyagramı, SCZ hastalarının Brodmann alanı 9'unda ve dışkı mikrobiyomuyla nakledilen farelerin beyinlerinde 7 örtüşen DEGen'in bulunduğunu ve SCZ hastalarının Brodmann alanı 24'ünde ve dışkı mikrobiyomuyla nakledilen farelerin beyinlerinde 4 örtüşen DEGen'in bulunduğunu gösterdi (Şekil 6A). Tüm bu üç grup arasında sadece 1 örtüşen DEGen bulundu (Şekil 6A). Farklı iki grup arasında bulunan tüm bu farklı ortak ifade genleri arasında Cybb, Gabre, Cartpt, Ifitm1, Baiap3, Arhgap36, Col4a3, Magel2, Ppef1 ve Rsad2 yer almaktadır (Şekil 6B ve Tablo S6). Önemli ölçüde zenginleştirilmiş en üst KEGG yolları esasen GABAerjik sinaps, Ferroptosis, HIF-1 sinyal yolu, Nöroaktif ligand-reseptör etkileşimi ve nörodejenerasyon yolları içermekteydi (Şekil 6C).
FMT farelerinde zenginleştirilmiş veya azalmış mikropların beyindeki farklı genlerle ilişkilendirilmesi
Daha sonra, FMT fare mikrobiyomunu ilişkili beyin transkriptomlarıyla birleştirdik.
Değiştirilmiş bağırsak mikrobiyom cinsleri ile değiştirilmiş genler arasındaki kovaryasyonu değerlendirmek için Şekil 7'de bir korelasyon ısı haritası oluşturuldu. Spearman korelasyon analizi, çoğu DEGen'in Lactobacillus, Alistipes, Bacteroides ve Christensenella ile pozitif korelasyon gösterdiğini, Helicobacter, Ruminococcaceae_UCG-010, Odoribacter, Paraprevotella ve Catabacter ile ise negatif korelasyon gösterdiğini ortaya koydu (Şekil 7). Dikkat çekici olarak, yukarıdaki on örtüşen iltihaplanma ile ilişkili genin dört tanesi (Şekil 6B), Cybb, Gabre, Baiap3 ve Magel2, iki FMT fare grubu arasında 12 farklı cins ile ilişkili bulundu (Şekil 7). İlginçtir ki, Paraprevotella ve Catabacter'ın bolluğu Gabre, Baiap3 ve Magel2 seviyeleri ile pozitif, Cybb seviyeleriyle negatif korelasyon gösterdi (p<0,05; Şekil 7). Birlikte alınan sonuçlar, SCZ'li hastalardan bağırsak mikrobiyomunun nakledilmesinin fare modellerinde gen ekspresyonunu etkileyebileceğini göstermektedir. Gabre, Baiap3, Magel2 ve Cybb, SCZ araştırmaları için olası gelecek hedeflerdir.
Artan kanıtlar, bağırsak mikrobiyomunun beyin gelişimi ve davranışıyla bağlantılı olduğunu göstermektedir. Ve disbiyotik bağırsak mikrobiyomu, SCZ, Otizm Spektrum Bozukluğu (OSB) ve nörodejeneratif hastalıklar dahil olmak üzere çeşitli ruhsal bozukluklara yatkınlık sağlar31. Çalışmamız, SCZ'li hastalar ile sağlıklı kontroller arasında anlamlı bağırsak mikrobiyomu değişiklikleri buldu ve SCZ'li hastalarda daha düşük mikrobiyal çeşitlilik ve disbiyotik mikrobiyom bileşimi tespit edildi (Şekil 1). Dahası, SCZ'li hastalardan alınan dışkı mikrobiyomuyla nakledilen fareler SCZ benzeri davranışlar sergileyebilir. Ayrıca, SCZ'li hastalardan alınan dışkı mikrobiyomuna sahip farelerde, Nöroaktif ligand-reseptör etkileşimi, iltihaplanma ve bağışıklık ile ilgili sinyal yollarında transkript bozuklukları bulduk, bunlar SCZ patolojisi ile güçlü bir şekilde ilişkilidir. Ek olarak, bütünleştirilmiş dizileme verisi analizi, SCZ hastaları ve dışkı mikrobiyomuna sahip fareler arasında örtüşen DEGenlerin esas olarak GABAerjik sinaps ve iltihaplanma ile ilgili sinyal yollarında zenginleştirildiğini gösterdi. Sonuçlarımız, bağırsak mikrobiyomu ve beyindeki iltihaplanma ile ilişkili genlerin SCZ patolojisindeki temel işlevsel rollerini desteklemektedir.
Kontrol gruplarına kıyasla, SCZ'li hastalarda mikrobiyom çeşitliliği düşük oldu (Şekil 1A), bu da önceki çalışmalar13,32 ile uyumlu. Mikrobiyal topluluk bileşimi ve SCZ'li hastalarda ve kontrol gruplarındaki bakteri bollukları, çalışmamız ile önceki çalışma arasında tutarsızlık göstermektedir. Çalışmamızda Shigella ve Collinsella SCZ'li hastalarda daha fazla, Faecalibacterium, Coprococcus, Prevotella, Haemophilus, Ruminococcaceae_Ruminococcus, Bacteroides ve Oscillospira ise kontrol gruplarında daha fazla bulundu (Şekil 1). Ancak Zheng vd.'nin13 çalışmasında, Megasphera, Akkermansia, Fusobacterium ve Prevotella SCZ'li hastalarda, Citrobacter, Blautia, Coprococcus ve Lachnoclostridium ise kontrol gruplarında daha fazla bulundu. Bu tutarsızlıklar, sigara içimi, antipsikotik tedavi ve metabolik hastalıklar gibi olası karıştırıcı faktörlerin hariç tutulmasıyla ilişkilendirilebilir, tüm bunlar mikrobiyomu etkiler. Sigara içimi ve diğer metabolik hastalıkları olan bazı denekler çalışmamızda dışlandı; Zheng vd.'nin çalışmasında ise bir aydan önce herhangi bir antibiyotik, probiyotik ve prebiyotik kullanan, başka ruhsal hastalıkları olan örnekler dışlandı13.
Zhu vd.'nin ve Zheng vd.'nin yakın tarihli çalışmaları, SCZ mikrobiyomuyla nakledilen farelerde SC