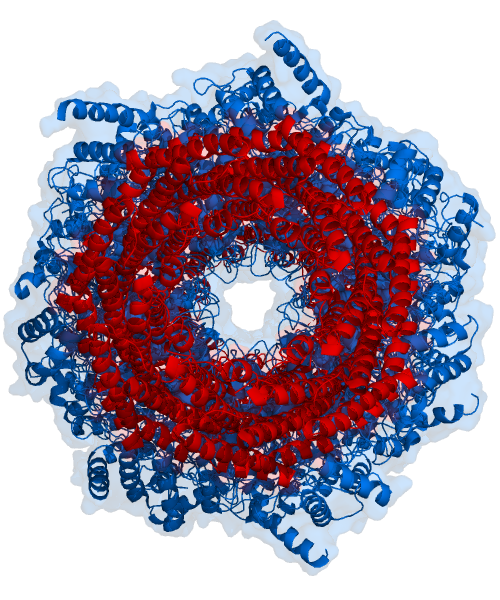
Bugün öğrendim ki: hücreler, yeniden katlanamayan yanlış katlanmış proteinleri alıp daha küçük alt birimlere ayıran proteazom adı verilen bir protein makinesi içerir. Ubiquitinlerin yanlış katlanmış proteinleri tespit edip proteazoma gönderdiği ubiquitin-proteazom adı verilen bir sistemin parçasıdır.
Übikitin etiketli proteinleri proteoliz yoluyla parçalayan protein kompleksleri.
Proteazomlar, peptit bağlarını kıran bir kimyasal reaksiyon olan proteoliz yoluyla übikitin etiketli proteinleri parçalayan protein kompleksleridir. Bu tür reaksiyonlara yardımcı olan enzimlere proteaz denir.
Proteazomlar, hücrelerin belirli proteinlerin konsantrasyonunu düzenlediği ve yanlış katlanmış proteinleri parçaladığı ana bir mekanizmanın parçasıdır. Proteinler, übikitin adı verilen küçük bir proteinle bozunmaya işaretlenir. Etiketleme reaksiyonu, übikitin ligazları adı verilen enzimler tarafından katalize edilir. Bir protein tek bir übikitin molekülü ile etiketlendiğinde, bu diğer ligazlara ek übikitin molekülleri eklemeleri için bir sinyaldir. Sonuç, proteazom tarafından bağlanan ve etiketlenmiş proteinin bozulmasını sağlayan poliübikitin zinciridir. [1] Bozunma süreci, yaklaşık yedi ila sekiz amino asit uzunluğunda peptitler üretir, bunlar daha sonra daha kısa amino asit dizilerine parçalanabilir ve yeni proteinlerin sentezinde kullanılabilir. [1]
Proteazomlar, tüm ökaryotlarda ve arkelerde ve bazı bakterilerde bulunur. Ökaryotlarda proteazomlar hem çekirdekte hem de sitoplazmada bulunur. [2]
Yapı olarak proteazom, merkezi bir gözenek oluşturan dört yığılmış halkadan oluşan "çekirdek" içeren silindirik bir komplekstir. Her halka yedi bireysel proteinden oluşur. İçteki iki halka, üç ila yedi proteaz aktif bölgesi içeren yedi β alt biriminden oluşur. Bu bölgeler halkaların iç yüzeyinde bulunur, bu nedenle hedef protein bozunmadan önce merkezi gözeneğe girmelidir. Dıştaki iki halka, her biri yedi α alt biriminden oluşur ve işlevi, proteinlerin varil içine girdiği "kapı"yı korumaktır. Bu α alt birimleri, protein substratlarına bağlı poliübikitin etiketlerini tanıyan ve bozunma sürecini başlatan "kapak" yapılarına veya düzenleyici partiküllere bağlanarak kontrol edilir. Übikitinasyon ve proteazomal bozunma genel sistemi, übikitin-proteazom sistemi olarak bilinir. [3]
Proteazomal bozunma yolu, hücre döngüsü, gen ifadesinin düzenlenmesi ve oksidatif strese yanıtlar dahil olmak üzere birçok hücresel süreç için çok önemlidir. Hücreler içindeki proteolitik bozunmanın önemi ve proteolitik yollarda übikitin rolü, 2004 Kimya Nobel Ödülü'nü Aaron Ciechanover, Avram Hershko ve Irwin Rose'a kazandırdı. [4]
Keşif
[değiştir]
Übikitin-proteazom sisteminin keşfinden önce, hücrelerdeki protein bozunumunun çoğunlukla lizozomlara, asidik ve proteaz dolu iç kısımları olan ve daha sonra ekzojen proteinleri ve yaşlı veya hasarlı organelleri parçalayabilen ve geri dönüştürebilen zarla çevrili organellere dayandığı düşünülüyordu. [1] Ancak, lizozomdan yoksun olan retikulositlerde ATP'ye bağımlı protein bozunumu üzerine Joseph Etlinger ve Alfred L. Goldberg'in 1977'de yaptığı çalışma, ikinci bir hücre içi bozunma mekanizmasının varlığını gösterdi. [5] Bunun 1978'de o zamanki proteazlar arasında bir yenilik olan birkaç farklı protein zincirinden oluştuğu gösterildi. [6] Daha sonra histonların modifikasyonu üzerine yapılan çalışmalar, histon proteininin beklenmedik bir kovalent modifikasyonunu, histonun bir lizin yan zincirinin übikitin, bilinmeyen bir işlevi olan bir proteinin C-terminal glisin kalıntısıyla bir bağ yoluyla modifikasyonunu ortaya çıkardı. [7] Daha sonra, daha önce proteolitik bozunma ile ilişkili olarak tanımlanmış bir protein olan ATP'ye bağımlı proteoliz faktörü 1 (APF-1)'in übikitin ile aynı protein olduğu keşfedildi. [8] Bu sistemin proteolitik aktiviteleri, başlangıçta Sherwin Wilk ve Marion Orlowski tarafından çoklu katalitik proteinaz kompleksi olarak adlandırılan çoklu protein kompleks olarak izole edildi. [9] Daha sonra, übikitin'e bağımlı protein bozunumundan sorumlu olan ATP'ye bağımlı proteolitik kompleks keşfedildi ve 26S proteazomu olarak adlandırıldı. [10] [11]
Übikitin proteazom sisteminin keşfine yol açan erken çalışmaların çoğu, 1970'lerin sonlarında ve 1980'lerin başlarında Avram Hershko'nun laboratuvarında Technion'da gerçekleşti, burada Aaron Ciechanover lisansüstü öğrenci olarak çalışıyordu. Hershko'nun Fox Chase Kanser Merkezi'nde Irwin Rose'un laboratuvarında bir yıllık sabatik izni, önemli kavramsal içgörüler sağladı, ancak Rose daha sonra keşifteki rolünü küçümsedi. [12] Üçü, bu sistemi keşfettikleri için 2004 Kimya Nobel Ödülü'nü paylaştılar. [4]
Proteazomun yığılmış halka yapısını ortaya koyan elektron mikroskopisi verileri 1980'lerin ortalarında kullanılabilir hale gelmesine rağmen, [13] proteazom çekirdek parçacığının ilk yapısı, X ışını kristalografisi ile 1994 yılına kadar çözülmedi. [14] 2018'de, kriyojenik elektron mikroskopisi ile poliübikitinlenmiş bir protein substratı ile kompleksteki insan 26S proteazomunun ilk atomik yapıları çözüldü ve substratın nasıl tanındığını, deübikitinasyonunu, katlanmamış halini ve insan 26S proteazomu tarafından nasıl parçalandığını ortaya koydu. [15]
Yapı ve organizasyon
[değiştir]
Proteazom alt bileşenlerine genellikle Svedberg çökeltme katsayıları (S ile gösterilir) ile atıfta bulunulur. Memelilerde en çok kullanılan proteazom, yaklaşık 2000 kilodalton (kDa) moleküler kütleye sahip sitozolik 26S proteazomudur, bir 20S protein alt birimi ve iki 19S düzenleyici kapak alt birimi içerir. Çekirdek boştur ve proteinlerin bozunduğu kapalı bir boşluk sağlar; çekirdeğin iki ucundaki açıklıklar, hedef proteinin içeri girmesini sağlar. Çekirdek parçacığının her iki ucu, birden fazla ATPaz aktif bölgesi ve übikitin bağlama bölgesi içeren 19S düzenleyici bir alt birimi ile birleşir; poliübikitinlenmiş proteinleri tanıyan ve katalitik çekirdeğe aktaran bu yapıdır. [15] 19S parçacığı ile aynı şekilde çekirdeğe bağlanabilen 11S parçacığı adı verilen alternatif bir düzenleyici alt birim formu; 11S, bir virüs tarafından enfeksiyondan sonra üretilenler gibi yabancı peptitlerin bozunmasında rol oynayabilir. [16]
20S çekirdek parçacığı
[değiştir]
"20S" buraya yönlendiriliyor. On yıl için bkz. 20'ler.
20S çekirdek parçacığında bulunan alt birimlerin sayısı ve çeşitliliği organizmaya bağlıdır; farklı ve özelleşmiş alt birimlerin sayısı, tek hücreli organizmalardan çok hücreli organizmalarda daha fazla ve prokaryotlardan ökaryotlarda daha fazladır. Tüm 20S parçacıkları, kendileri iki farklı alt birim türünden oluşan dört yığılmış heptamerik halka yapısından oluşur; α alt birimleri yapısal doğadadır, β alt birimleri ise ağırlıklı olarak katalitiktir. α alt birimleri, β alt birimlerine homolog olan psödoenzimlerdir. N-uçları, β alt birimlerinin N-uçlarına bitişik olacak şekilde birleştirilirler. [17] Yığındaki dıştaki iki halka, her biri yedi α alt biriminden oluşur ve düzenleyici partiküller için yanaşma bölgeleri görevi görür ve alfa alt birimlerinin N-uçları (Pfam PF10584), substratların iç boşluğa düzenlenmemiş erişimini engelleyen bir kapı oluşturur. [18] İçteki iki halka, her biri yedi β alt biriminden oluşur ve N-uçlarında, proteoliz reaksiyonlarını gerçekleştiren proteaz aktif bölgeleri bulunur. [19] Saflaştırılmış komplekste üç farklı katalitik aktivite tanımlandı: kimotripsin benzeri, tripsin benzeri ve peptidilglutamil-peptit hidrolize eden. [20] Proteazomun boyutu nispeten korunmuştur ve yaklaşık 150 angstrom (Å) x 115 Å'dir. İç odanın genişliği en fazla 53 Å'dir, ancak giriş 13 Å kadar dar olabilir, bu da substrat proteinlerinin içeri girmek için en azından kısmen katlanmamış olması gerektiğini göstermektedir. [21]
Thermoplasma acidophilum gibi arkelerde, tüm α ve tüm β alt birimleri özdeştir, oysa maya gibi ökaryotik proteazomlar, her alt birimden yedi farklı tip içerir. Memelilerde, β1, β2 ve β5 alt birimleri katalitiktir; ortak bir mekanizmayı paylaşsalar da, kimotripsin benzeri, tripsin benzeri ve peptidil-glutamil peptit hidrolize eden (PHGH) olarak kabul edilen üç farklı substrat özgüllüğüne sahiptirler. [22] β1i, β2i ve β5i olarak adlandırılan alternatif β formları, sitokinler, özellikle interferon gama gibi proinflamatuar sinyallere maruz kalma karşılık olarak hematopoetik hücrelerde ifade edilebilir. Bu alternatif alt birimlerle birleştirilmiş proteazom, immunoproteazom olarak bilinir ve substrat özgüllüğü normal proteazomun özgüllüğünden farklıdır. [21] Son zamanlarda, insan hücrelerinde α3 çekirdek alt birimi eksik olan alternatif bir proteazom tanımlandı. [23] Bu proteazomlar (α4-α4 proteazomları olarak bilinir), eksik α3 alt biriminin yerine ek bir α4 alt birimi içeren 20S çekirdek parçacıkları oluştururlar. Bu alternatif 'α4-α4' proteazomları, daha önce mayada var olduğu bilinmektedir. [24] Bu proteazom izoformlarının kesin işlevi hala büyük ölçüde bilinmemekle birlikte, bu proteazomları ifade eden hücreler, kadmiyum gibi metal iyonları tarafından indüklenen toksisiteye karşı artan direnç göstermektedir. [23] [25]
19S düzenleyici parçacığı
[değiştir]
Ökaryotlardaki 19S parçacığı, 19 bireysel proteinden oluşur ve 20S çekirdek parçacığının α halkasına doğrudan bağlanan 9 alt birimli bir baz ve 10 alt birimli bir kapak olmak üzere iki alt topluluğa ayrılabilir. Dokuz baz proteininden altısı, AAA Ailesinden ATPaz alt birimleridir ve bu ATPazların evrimsel bir homologu, arkelerde PAN (proteazom aktive edici nükleotidaz) olarak bulunur. [26] 19S ve 20S parçacıklarının birleşmesi, 19S ATPaz alt birimlerine ATP bağlanmasını gerektirir ve ATP hidrolizi, birleştirilmiş kompleks tarafından katlanmış ve übikitinlenmiş proteinleri bozmak için gereklidir. Sadece substrat katlanmamış halinin ATP hidrolizinden gelen enerjiye ihtiyaç duyduğunu, ATP bağlanmasının tek başına protein bozunması için gerekli diğer tüm adımları destekleyebileceğini (örneğin, kompleks montajı, kapı açılması, translokasyon ve proteoliz) unutmayın. [27] [28] Aslında, ATPazlara ATP bağlanması kendi başına, katlanmamış proteinlerin hızlı bozunmasını destekler. Ancak, ATP hidrolizi sadece katlanmamış hale getirmek için gerekli iken, bu enerjinin bu adımların bazılarının birleştirilmesinde kullanılıp kullanılmadığı henüz net değil. [28] [29]
2012 yılında, iki bağımsız çalışma, 26S proteazomunun moleküler mimarisini tek parçacık elektron mikroskopisi ile açıkladı. [31] [32] 2016 yılında, üç bağımsız çalışma, insan 26S proteazomunun substrat bulunmayan halinin ilk atomik çözünürlüğe yakın yapısını cryo-EM ile belirledi. [33] [34] [35] 2018 yılında, büyük bir çalışma, yedi atomik yapı belirleyerek, substrata bağlı 26S proteazomunun deübikitinasyonunu, translokasyonun başlamasını ve substratın işlenen katlanmamış halini, aynı anda, detaylı mekanizmalarını açıkladı. [15] 19S'in kalbinde, doğrudan 20S'nin yanına, Rpt1/Rpt2/Rpt6/Rpt3/Rpt4/Rpt5 sırasıyla heterohekzamerik bir halkaya birleşen AAA-ATPazlar (AAA proteinleri) bulunur. Bu halka, Rpt1/Rpt2, Rpt6/Rpt3 ve Rpt4/Rpt5'in N-terminal kıvrımlı-sarmal yapıları aracılığıyla dimerleştiği, bir üçlü dimerdir. Bu kıvrımlı-sarmal yapılar, hekzanerik halkadan dışarı çıkar. En büyük düzenleyici parçacık olmayan ATPazlar olan Rpn1 ve Rpn2, sırasıyla Rpt1/2 ve Rpt6/3'ün uçlarına bağlanır. Übikitin reseptörü Rpn13, Rpn2'ye bağlanır ve baz alt kompleksini tamamlar. Kapak, AAA-ATPaz hekzanerinin (Rpt6/Rpt3/Rpt4) yarısını örter ve beklenmedik bir şekilde, Rpn6 aracılığıyla doğrudan 20S'ye ve daha az ölçüde Rpn5'e temas eder. Yapısal olarak birbirlerine ve COP9 kompleksi ve eIF3'ün alt birimlerine (bu nedenle PCI alt birimleri olarak adlandırılır) bağlı olan Rpn9, Rpn5, Rpn6, Rpn7, Rpn3 ve Rpn12 alt birimleri, Rpn8/Rpn11 heterodimerini kaplayan, at nalı benzeri bir yapıya birleşir. Deübikitinasyon enzimi olan Rpn11, AAA-ATPaz hekzanerinin ağzına yerleştirilir ve substratların 20S'ye translokasyonundan hemen önce übikitin kalıntıları kaldırabilecek ideal bir konumdadır. Bugüne kadar tanımlanmış ikinci übikitin reseptörü olan Rpn10, Rpn8 ve Rpn9 alt birimlerinin yakınında, kapağın çevresine yerleştirilir.
19S'nin konformasyonel değişiklikleri
[değiştir]
26S proteazom holoenzimi içindeki 19S düzenleyici parçacığı, bugüne kadar substrat bulunmayan halde altı farklı konformasyonel durumda gözlemlenmiştir. [36] [37] AAA-ATPaz konfigürasyonunun bu baskın düşük enerjili durumdaki bir özelliği, AAA-bölgelerinin merdiven benzeri veya kilit yıkama benzeri bir düzenlemesidir. [30] [31] ATP varlığında ancak substrat yokluğunda, 19S'in üç alternatif, daha az bol konformasyonu benimsenir, öncelikle kapak pozisyonunun AAA-ATPaz modülüne göre farklı olmasıyla. [33] [37] ATP-γS veya bir substrat varlığında, AAA-ATPaz modülünün önemli yapısal değişikliklerini gösteren önemli ölçüde daha fazla konformasyon gözlemlenmiştir. [15] [36] [38] [39] Substrata bağlı konformasyonların bazıları substratsız olanlara yüksek benzerlik gösterir, ancak özellikle AAA-ATPaz modülünde tamamen aynı değildir. [15] [36] 26S montajından önce, serbest formda 19S düzenleyici parçacığı da yedi konformasyonel durumda gözlemlenmiştir. [40] Önemli olarak, tüm bu konformerler bir şekilde farklıdır ve farklı özellikler gösterir. Bu nedenle, 19S düzenleyici parçacığı, farklı fizyolojik koşullar altında en az 20 konformasyonel durumu örnekleme yeteneğine sahiptir.
19S tarafından 20S'nin düzenlenmesi
[değiştir]
19S düzenleyici parçacığı, 20S'yi proteinleri bozması için uyarlamaktan sorumludur. 19S düzenleyici ATPazların birincil işlevi, substratların bozunma odasına girmesini engelleyen 20S'deki kapıyı açmaktır. [41] Proteazomal ATPazların bu kapıyı nasıl açtığı mekanizması son zamanlarda açıklığa kavuşturuldu. [18] 20S kapısının açılması ve dolayısıyla substrat bozunumu, belirli bir motif (yani HbYX motifi) içeren proteazomal ATPazların C-uçlarını gerektirir. ATPazların C-uçları, 20S'nin tepesindeki ceblere bağlanır ve ATPaz kompleksini 20S proteolitik kompleksiyle bağlar, böylece substratı katlanmamış hale getirme ekipmanını 20S bozunma mekanizmasıyla birleştirir. Bu C-uçlarının kendi başına bu 20S ceblerine bağlanması, 20S'deki kapının "bir kilitte anahtar"ın bir kapıyı açmasıyla aynı şekilde açılmasını uyarır. [18] Bu "bir kilitte anahtar" mekanizmasının tam olarak nasıl işlediği mekanizması, insan 26S proteazomunun bağlamında atomik çözünürlüğe yakın bir şekilde yapısal olarak açıklığa kavuşturuldu ve ATPaz alt birimleri Rpt1/2/3/5/6'nın beş C-ucunun 20S yüzey ceblerine girmesinin 20S kapısını tamamen açmak için gerekli olduğunu göstermektedir. [36] [15] [33]
Diğer düzenleyici partiküller
[değiştir]
"11S" buraya yönlendiriliyor. S11 veya 11 (çoğul) ile karıştırılmamalıdır.
20S proteazomları, herhangi bir ATPaz içermeyen ve tam proteinlerin değil, kısa peptitlerin bozunmasını sağlayabilen, heptamerik bir yapı olan ikinci bir düzenleyici parçacık türü olan 11S düzenleyici parçacığı ile de birleşebilir. Bunun nedeni, kompleks daha büyük substratları katlanmamış hale getiremeyebilir. Bu yapı aynı zamanda PA28, REG veya PA26 olarak da bilinir. [17] Çekirdek parçacığına alt birimlerinin C-terminal kuyrukları aracılığıyla nasıl bağlandığı ve 20S kapısını açmak için α halkasının konformasyonel değişikliklerini indüklediği mekanizmaları, 19S parçacığı için benzer bir mekanizmayı göstermektedir. [42] 11S parçacığının ifadesi interferon gama tarafından indüklenir ve ana histokompatibilite kompleksi'ne bağlanan peptitlerin üretilmesinden sorumludur. [16]
ATPaz olmayan düzenleyici parçacıkların bir diğer türü ise Blm10 (maya) veya PA200/PSME4 (insan)dır. Sadece 20S kapısındaki bir α alt birimini açar ve kendisi üzerinde çok küçük bir gözeneğe sahip bir kubbeye katlanır. [17]
Montaj
[değiştir]
Proteazomun montajı, aktif bir kompleks oluşturmak için bir araya gelmesi gereken alt birim sayısı nedeniyle karmaşık bir işlemdir. β alt birimleri, 20S parçacığının montajı sırasında post-translasyonel olarak modifiye edilen ve proteolitik aktif bölgeyi ortaya çıkaran N-terminal "propeptitler" ile sentezlenir. 20S parçacığı, her biri yedi üyeli bir pro-β halkasının yedi üyeli bir α halkasına bağlandığı iki yarı-proteazomdan birleştirilir. İki yarı-proteazomun β halkalarının birleşmesi, aktif bölgeyi ortaya çıkarmak için propeptitlerin treonin'e bağımlı otolizini tetikler. Bu β etkileşimleri, mutasyonlar tarafından bozulması proteazomun bir araya gelme yeteneğine zarar veren, korunmuş alfa sarmal yapıları arasındaki tuz köprüleri ve hidrofobik etkileşimler tarafından esas olarak aracılık edilir. [43] Yarı-proteazomların montajı, α alt birimlerinin heptamerik halkalarına birleşmesiyle başlatılır ve karşılık gelen pro-β halkasının birleşmesi için bir şablon oluşturur. α alt birimlerinin birleşmesi karakterize edilmemiştir. [44]
Sadece son zamanlarda, 19S düzenleyici parçacığının montaj süreci önemli ölçüde açıklığa kavuşturuldu. 19S düzenleyici parçacığı, baz ve kapak olmak üzere iki farklı alt bileşen olarak bir araya gelir. Baz kompleksinin montajı, dört montaj şaperonu tarafından kolaylaştırılır: Hsm3/S5b, Nas2/p27, Rpn14/PAAF1 ve Nas6/gankyrin (maya/memeliler için isimler). [45] Bu montaj şaperonları, AAA-ATPaz alt birimlerine bağlanır ve ana işlevleri, heterohekzamerik AAA-ATPaz halkasının doğru bir şekilde birleştirilmesini sağlamak gibi görünmektedir. Bugüne kadar, baz kompleksinin ayrı bir şekilde bir araya gelip gelmediği, montajın 20S çekirdek parçacığı tarafından şablonlanıp şablonlanmadığı veya alternatif montaj yollarının olup olmadığı hala tartışılıyor. Dört montaj şaperonuna ek olarak, deübikitinasyon enzimi Ubp6/Usp14 da baz montajını destekler, ancak bu işlem için olmazsa olmaz değildir. [46] Kapak, ayrı olarak belirli bir sırada bir araya gelir ve montaj şaperonlarına ihtiyaç duymaz. [47]
Protein bozunma süreci
[değiştir]
Übikitinasyon ve hedefleme
[değiştir]
Daha fazla bilgi: Übikitin § Übikitinasyon
Proteinler, üç enzimin koordine edilmiş reaksiyonlarını gerektiren bir lizin kalıntısının kovalent modifikasyonu ile proteazom tarafından bozunmaya hedeflenir. İlk adımda, bir übikitin aktive edici enzim (E1 olarak bilinir), ATP'yi hidrolize eder ve bir übikitin molekülünü adenilize eder. Bu daha sonra, ikinci bir übikitin adenilize edilmesiyle birlikte E1'in aktif bölge sistein kalıntısına aktarılır. [48] Bu adenilize edilmiş übikitin daha sonra ikinci bir enzim olan übikitin konjugasyon enzimi (E2)'nin bir sisteinine aktarılır. Son adımda, übikitin ligazları (E3) olarak bilinen çok çeşitli bir enzim sınıfından bir üye, übikitinlenecek özel proteini tanır ve übikitin'in E2'den bu hedef proteine aktarılmasını katalize eder. Bir hedef protein, proteazom kapağı tarafından tanınmadan önce en az dört übikitin monomeriyle (poliübikitin zinciri şeklinde) etiketlenmelidir. [49] Bu nedenle, E3 bu sisteme substrat özgüllüğünü kazandırır. [50] İfade edilen E1, E2 ve E3 proteinlerinin sayısı organizmaya ve hücre türüne bağlıdır, ancak insanlarda çok sayıda farklı E3 enzimi bulunur, bu da übikitin proteazom sistemi için çok sayıda hedef olduğunu göstermektedir.
Poliübikitinlenmiş bir proteinin proteazoma nasıl hedeflendiği tam olarak anlaşılamamıştır. Poliübikitinlenmiş proteine bağlı proteazomun birkaç yüksek çözünürlüklü anlık görüntüsü, übikitin reseptörlerinin başlangıçta substrat hedeflemesi ve tutunması için deübikitinasyon enzimi Rpn11 ile koordine edilebileceğini düşündürmektedir. [15] Übikitin reseptör proteinleri, N-terminal übikitin benzeri (UBL) bir domaine ve bir veya daha fazla übikitin ile ilişkili (UBA) domaine sahiptir. UBL alanları, 19S proteazom kapakları tarafından tanınır ve UBA alanları, üç-sarmal demetleri aracılığıyla übikitin'e bağlanır. Bu reseptör proteinleri, poliübikitinlenmiş proteinleri proteazoma eşlik edebilir, ancak bu etkileşimin ayrıntıları ve düzenlenmesi net değildir. [51]
Übikitin proteini, 76 amino asit uzunluğunda olup, yüksek oranda korunmuş bir diziye sahip olduğu ve tüm bilinen ökaryotik organizmalarda bulunduğu için adı buradan geliyor. [52] Ökaryotlarda übikitin'i kodlayan genler, muhtemelen hücrenin ürettiği yeterli übikitin'i üretmek için bu genlere olan yoğun transkripsiyon talebinden dolayı tandem tekrarlar halinde düzenlenir. Übikitin'in bugüne kadar tanımlanmış en yavaş evrimleşen protein olduğu öne sürülmüştür. [53] Übikitin, başka bir übikitin'in bağlanabileceği yedi lizin kalıntısı içerir ve bu da farklı poliübikitin zinciri türleri oluşturur. [54] Her ek übikitin, önceki übikitin'in lizin 48'ine bağlandığı zincirler, proteazom hedeflemesinde rol oynar, diğer zincir türleri ise diğer süreçlerde yer alabilir. [55] [56]
Deübikitinasyon
[değiştir]
Proteazomal bozunmaya hedeflenen bir proteine konjuge edilen übikitin zincirleri normalde, Rpn11, Ubp6/USP14 ve UCH37 olan üç proteazomla ilişkili deübikitinasyon enzimi (DUB)'nden biri tarafından çıkarılır. Bu işlem, übikitin'i geri dönüştürür ve hücrelerdeki übikitin rezervuarını korumak için çok önemlidir. [56] Rpn11, 19S düzenleyici parçacığının içsel, stokiyometrik bir alt birimidir ve 26S proteazomunun işlevi için çok önemlidir. Rpn11'in DUB aktivitesi, monomerik formuna kıyasla proteazomda artar. Rpn11'in bir protein substratından bir übikitin zincirini nasıl bir bütün olarak kaldırdığı, EB adı verilen bir konformasyonda substrata bağlı insan proteazomunun atomik yapısı tarafından yakalandı. [15] İlginç bir şekilde, bu yapı ayrıca DUB aktivitesinin proteazomal AAA-ATPaz tarafından substrat tanıma ile nasıl bağlantılı olduğunu da göstermektedir. Rpn11'in aksine, USP14 ve UCH37, her zaman proteazomla ilişkili olmayan DUB'lardır. Hücrelerde, proteazomların yaklaşık %10-40'ının USP14 ile ilişkili olduğu bulundu. Hem Ubp6/USP14 hem de UCH37, büyük ölçüde proteazom tarafından aktive edilir ve tek başına çok düşük bir DUB aktivitesi sergiler. Aktive edildiğinde, USP14'ün DUB aktivitesiyle ve proteazom konformasyonel geçişlerinin paralel yollarını indükleyerek proteazom işlevini bastırdığı bulundu, bunlardan birinin de AAA-ATPaz'a substrat girişini doğrudan engellediği, zaman çözümlü kriyojenik elektron mikroskopisi ile sezgisel olarak gözlemlendiği gibi. [57] Görünüşe göre USP14, hem katalitik olarak Rpn11 ile rekabet ederek hem de AAA-ATPaz durumlarını allosterik olarak yeniden programlayarak proteazom işlevini birden fazla kontrol noktasında düzenler, bu da bir DUB için oldukça beklenmedik bir durumdur. [57] Bu gözlemler, proteazom düzenlemesinin konformasyonel durumlarının dinamik geçişlerine bağlı olabileceğini ima eder.
Katlanmamış hale getirme ve translokasyon
[değiştir]
Bir protein übikitinlendikten sonra, ATP'ye bağımlı bir bağlanma adımında 19S düzenleyici parçacığı tarafından tanınır. [15] [28] Daha sonra, substrat proteini, proteolitik aktif bölgelere temas etmek için 20S alt biriminin içine girmelidir. 20S parçacığının merkezi kanalı dar olduğu ve α halkası alt birimlerinin N-terminal kuyrukları tarafından kapılı olduğu için, substratlar çekirdeğe girmeden önce en azından kısmen katlanmamış hale getirilmelidir. [15] Katlanmamış substratın çekirdeğe geçişi translokasyon olarak adlandırılır ve deübikitinasyon işleminden sonra mutlaka gerçekleşir. [15] [28] Ancak, substratların hangi sırayla deübikitinlendiği ve katlanmamış hale getirildiği henüz net değil. [58] Bu işlemlerden hangisinin genel proteoliz reaksiyonundaki hız sınırlayıcı adım olduğu, belirli substrata bağlıdır; bazı proteinler için katlanmamış hale getirme işlemi hız sınırlayıcıdır, oysa diğer proteinler için deübikitinasyon en yavaş adımdır. [27] Substratların translokasyondan önce ne kadar katlanmamış hale getirilmesi gerektiği, substrata bağlı 26S proteazomunun deübikitinasyon uyumlu durumunun atomik yapısı tarafından yaklaşık 20 amino asit kalıntısı olarak öneriliyor, [15] ancak önemli üçlü yapı ve özellikle disülfür bağları gibi yerel olmayan etkileşimler, bozunmayı engellemek için yeterlidir. [59] Protein terminalinde veya içsel olarak, yeterince büyük, içsel olarak düzenlenmemiş protein segmentlerinin varlığı, bozunmanın verimli bir şekilde başlatılmasını kolaylaştırmak için de önerilmiştir. [60] [61]
α alt birimleri tarafından oluşturulan kapı, yaklaşık dört kalıntıdan uzun peptitlerin 20S parçacığının içine girmesini önler. İlk tanıma adımından önce bağlanan ATP molekülleri, translokasyondan önce hidrolize edilir. Substratı katlanmamış hale getirmek için enerji gerekli olsa da, translokasyon için gerekli değildir. [27] [28] Birleştirilmiş 26S proteazomu, hidrolize edilemeyen bir ATP analoğu varlığında katlanmamış proteinleri bozabilir, ancak katlanmış proteinleri bozamaz, bu da ATP hidrolizinden gelen enerjinin substratı katlanmamış hale getirmek için kullanıldığını gösterir. [27] Katlanmamış substratın açılmış kapıdan geçişi, 19S kapak ATP ile bağlanmış durumda ise kolaylaştırılmış difüzyon yoluyla gerçekleşir. [62]
Küresel proteinlerin katlanmamış hale getirilme mekanizması, zorunlu olarak geneldir, ancak bir şekilde amino asit dizisine bağlıdır. Sıralı glisin ve alaninden oluşan uzun dizilerin, substrat katlanmamış halini engellediği, proteazomal bozunma verimliliğini azalttığı ve muhtemelen ATP hidrolizi ve katlanmamış hale getirme adımlarının ayrışması nedeniyle kısmen parçalanmış yan ürünlerin salınmasına yol açtığı gösterilmiştir. [63] Bu tür glisin-alanin tekrarları doğada da bulunur, örneğin ipek fibroin'de; özellikle, bu diziyi taşıyan bazı Epstein-Barr virüsü gen ürünleri proteazomu durdurabilir ve ana histokompatibilite kompleksinde antijen sunumunu önleyerek virüsün yayılmasına yardımcı olabilir. [64]
Proteoliz
[değiştir]
Ayrıca bkz: treonin proteaz § mekanizma
Proteazom, bir endoproteaz olarak işlev görür. [65] [66] [67] [68] 20S çekirdek parçacığının β alt birimleri tarafından proteoliz mekanizması, treonin'e bağımlı nükleofilik bir saldıri aracılığıyla gerçekleşir. Bu mekanizma, reaktif treonin hidroksilin deprotonasyonu için ilişkili bir su molekülüne bağlı olabilir. Bozunma, iki β halkasının birleşmesiyle oluşan merkezi odada gerçekleşir ve normalde kısmen parçalanmış ürünler salmaz, bunun yerine substratı genellikle 7-9 kalıntı uzunluğunda kısa polipeptitlere indirger, ancak organizmaya ve substrata bağlı olarak 4 ila 25 kalıntı arasında değişebilir. Ürün uzunluğunu belirleyen biyokimyasal mekanizma tam olarak karakterize edilmemiştir. [69] Üç katalitik β alt birimi ortak bir mekanizmaya sahip olsa da, kimotripsin benzeri, tripsin benzeri ve peptidil-glutamil peptit hidrolize eden (PHGH) benzeri olarak kabul edilen, biraz farklı substrat özgüllüklerine sahiptir. Bu özgüllükteki varyasyonlar, her alt birimin aktif bölgesinin yakınındaki yerel kalıntılarla atomik etkileşimlerin sonucudur. Her bir katalitik β alt birimi, proteoliz için gerekli olan korunmuş bir lizin kalıntısı da içerir. [22]
Proteazom normalde çok kısa peptit parçaları üretmesine rağmen, bazı durumlarda bu ürünler kendi başına biyolojik olarak aktif ve işlevsel moleküllerdir. Belirli genlerin ekspresyonunu düzenleyen bazı transkripsiyon faktörleri, memeli kompleks NF-κB'nin bir bileşenini içerir ve bunlar, übikitinasyonları ve ardından proteazomal bozunmaları tarafından aktif hale getirilen inaktif öncüler olarak sentezlenir. Bu tür aktivite, proteazomun substrat proteinini işlemsel olarak bir uçtan bozmak yerine, substrat proteinini içsel olarak kesmesini gerektirir. Bu proteinlerin yüzeylerindeki uzun döngülerin, proteazomal substratlar olarak hizmet ettiği ve merkezi boşluğa girdiği, proteinin büyük kısmının ise dışarıda kaldığı öne sürülmüştür. [70] Maya proteinlerinde benzer etkiler gözlemlenmiştir; bu seçici bozunma mekanizması, düzenlenmiş übikitin/proteazoma bağımlı işleme (RUP) olarak bilinir. [71]
Übikitin'e bağımsız bozunma
[değiştir]
Proteazomal substratların çoğu, bozunmadan önce übikitinlenmesi gerekmesine rağmen, özellikle proteazom proteinin post-translasyonel işlenmesinde normal bir rol oynadığında, bu genel kurala bazı istisnalar vardır. NF-κB'nin, p105'in iç proteoliz yoluyla p50'ye işlenmesiyle proteazomal aktivasyonu, en önemli örneklerden biridir. [70] İç